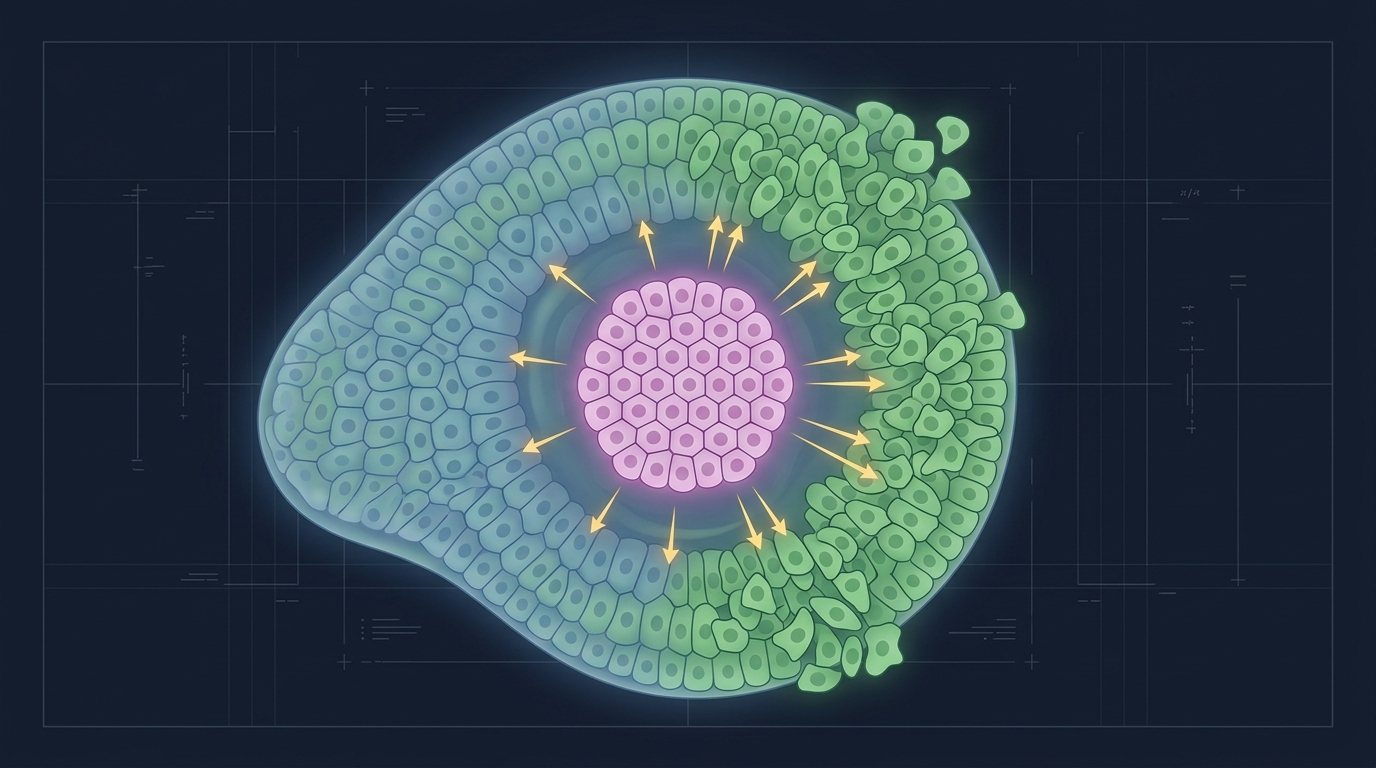
がんを止めるはずの遺伝子が、隣の細胞をがんに変える――広島大学の研究チームが、20年以上「がん抑制経路」として知られてきた Hippo 経路の、まったく逆の顔を捉えました。
ショウジョウバエの翅を舞台に明らかになったのは、「優等生な細胞」がひそかに周囲をがん化させる、新しい発がんのシナリオです。
広島大学・千原研究室らの研究チームが、がん抑制経路として研究されてきた Hippo 経路が、ショウジョウバエ翅原基の特定領域では逆に隣接細胞をがん化させる「発がんニッチ細胞」として働くことを EMBO Reports に発表した。
本研究は2026年5月1日に EMBO Reports(DOI: 10.1038/s44319-026-00778-5)に掲載され、Hippo が活性化した細胞が hinge/ventral notum 領域において Dronc–Wingless(Wg)/Spitz シグナリングを誘導し、隣接細胞で mTOR 経路を活性化することを示した。
研究チームは新規アミノ酸トランスポーター Sat1(CG4991)および Sat2(CG16700)を同定した。Sat1/Sat2 はヒトの SLC36A1〜4 ファミリーと相同で、Wg/Spitz と冗長に機能する。本論文に対する News & Views(DOI: 10.1038/s44319-026-00777-6)が同日公開された。
From: ![]() The Hippo tumor suppressor pathway triggers non-cell autonomous tumorigenesis in Drosophila
The Hippo tumor suppressor pathway triggers non-cell autonomous tumorigenesis in Drosophila
【編集部解説】
今回発表された研究結果は、がん研究の「常識」が反転したことを示すものです。
Hippo 経路はショウジョウバエで発見されて以来、20年以上にわたり「腫瘍抑制経路」の代表格として位置づけられてきました。世界中のがん研究において、Hippo の働きを取り戻すこと(つまり YAP/TAZ の活性を抑えること)は、有望な治療戦略の一つとして語られてきた経緯があります。
しかし本論文は、その枠組みを部分的に書き換えるものです。Hippo が活性化した細胞自身は一見「優等生」のように振る舞いながら、隣接する細胞にがん化のシグナルを送りつけている――この「非細胞自律的(non-cell autonomous)」という視点が、本研究の最大の革新性です。
非細胞自律的な腫瘍形成という考え方を、もう少し噛み砕いてみましょう。従来のがん研究は「変異を持った細胞そのものが暴走する」というモデルを基本としてきました。本論文はそれに対し「変異を持った細胞が、健全に見える周囲を巻き込んでがん化させる」という構図を提示しています。研究チームはこの細胞群を「発がんニッチ細胞(oncogenic niche cells)」と呼んでいます。
メカニズムも一筋縄ではいきません。Hippo 活性化細胞は、アポトーシス誘導因子である rpr、hid、grim を介して Dronc というカスパーゼを活性化し、Wg(Wingless)と Spitz という2つの増殖因子を分泌します。これに加え、本研究で新規に同定された2つのアミノ酸トランスポーター Sat1 と Sat2 が、メチオニンを含むアミノ酸の取り込みを担い、隣接細胞の mTOR 経路を活性化させて腫瘍化を促進する――という二段構えの仕掛けが見えてきました。
つまり Hippo が活性化した細胞は、自身の生存のためにアミノ酸を取り込み、その一部を周囲に放出することで、ある種の「がん促進的な微小環境」を能動的に作り出していると解釈できます。
もし Hippo 経路の活性化を「常に望ましい状態」として創薬を進めた場合、特定の組織や文脈ではかえって発がんを助長してしまう可能性が浮かび上がってきます。乳がんや血液がんでは過去にも YAP の喪失(すなわち Hippo 経路の活性化)が腫瘍進行に寄与する事例が報告されており、本研究はその分子メカニズムの一端を遺伝学的に裏付けたかたちです。
空間特異性も見逃せないポイントとなります。研究チームは、翅原基の中でも hinge(蝶番)および ventral notum(腹側胸背部)と呼ばれる特定の領域だけで、この発がんニッチが成立することを突き止めました。pouch(袋部)領域では同じ遺伝学的操作を行っても腫瘍化は起こりません。「同じ変異でも組織や部位によってがんになりやすさが違う」という臨床経験則に、分子レベルの説明を与えうる結果と言えるでしょう。
実用面では、Sat1/Sat2 のヒト相同体である SLC36A1〜4 ファミリーにも注目が集まる可能性があります。SLC36 ファミリーはアミノ酸輸送に関わるものの、がん微小環境との関係については未解明な点が多くありました。本研究によって、これらが「がんの微小環境」を支える重要な歯車であると示されたことで、新たな治療標的としての手がかりを提示したと言えます。
ただし、慎重に受け止めるべき点もあります。本研究はあくまでショウジョウバエの翅原基という発生中の上皮組織を用いた成果であり、哺乳類、ましてやヒトの成体組織で同じ機序がそのまま成立するかは今後の検証課題です。研究チーム自身も、これは「Hippo 経路ががん促進因子としても働きうる」というシナリオの一つを示したにすぎないと、抑制の効いた書きぶりを保っています。
それでも本研究が提示した「がんは細胞単独の暴走ではなく、近隣との対話の結果として起こりうる」という視座は、今後10年単位でがん研究の地平を広げていくはずです。Hippo 経路を標的とする治療薬は世界中で開発が進んでいますが、本知見は、その効果と副作用を組織特異性の観点から再評価する必要性を静かに突きつけています。
【用語解説】
Hippo 経路(ヒッポ経路)
ショウジョウバエで発見された、器官のサイズや細胞増殖を負に制御するシグナル伝達経路。1990年代以降に主要構成要素が段階的に同定されて以来、「がん抑制経路」の代表格として研究されてきた。
YAP / TAZ / Yorkie(Yki)
Hippo 経路の下流で働く転写共役因子。Hippo 経路が活性化されるとリン酸化されて細胞質に留まり、不活性化されると核内に移行して細胞増殖や生存に関わる遺伝子の発現を促す。Yorkie(Yki)はショウジョウバエでの呼称、YAP / TAZ はその哺乳類オルソログ。
非細胞自律的(non-cell autonomous)
ある細胞で起きた変化が、その細胞自身ではなく周囲の細胞に影響を及ぼす現象。今回の研究では、Hippo が活性化した細胞自身ではなく、その隣接細胞ががん化することを指す。
発がんニッチ細胞(oncogenic niche cells)
がん化を直接担うのではなく、周囲の細胞をがん化させる「土壌」として機能する細胞群。本研究で Hippo 活性化細胞がこの役割を果たすことが示された。
Wg(Wingless)/ Spitz
ショウジョウバエの増殖因子。Wg はヒトの Wnt のオルソログ、Spitz は EGF(上皮成長因子)のオルソログにあたる。今回の論文では、これらが Hippo 活性化細胞から分泌され、隣接細胞の増殖を促すことが示された。
Dronc
ショウジョウバエのイニシエーターカスパーゼ(細胞死を引き起こす酵素群の上流の一つ)。通常はアポトーシスを誘導するが、本研究では細胞死を起こさずに増殖シグナルを発する「非アポトーシス機能」を担うことが示された。
rpr / hid / grim
ショウジョウバエの3つの代表的なアポトーシス誘導遺伝子(reaper、head involution defective、grim)。Hippo 経路の活性化によって発現が上昇し、Dronc を活性化させる。
mTOR 経路
細胞の増殖や代謝、タンパク質合成を制御する中心的なシグナル伝達経路。アミノ酸が主要な活性化因子であり、多くのがんで過剰活性化が見られる。pS6(リン酸化リボソームタンパク質 S6)はその代表的な活性化マーカー。
Sat1 / Sat2
本研究で新規同定されたショウジョウバエのアミノ酸トランスポーター。正式遺伝子名は CG4991 および CG16700。ヒトの SLC36A1〜4 ファミリーと相同で、メチオニンを含むアミノ酸の細胞内取り込みに関与する。
SLC36 ファミリー
ヒトのプロトン共役型アミノ酸トランスポーターの一群。プロリンやアラニンなど特定のアミノ酸を輸送するが、機能の詳細は十分には解明されていない。
翅原基(はねげんき/wing disc)
ショウジョウバエの幼虫体内に存在する、成虫の翅と胸部の一部に分化する上皮組織。pouch(袋部・将来の翅)、hinge(蝶番・翅と胸の接合部)、notum(胸背部)の各領域から成り、本研究では領域ごとに異なる応答が観察された。
AiP(Apoptosis-induced Proliferation/アポトーシス誘導性増殖)
死にかけた細胞が周囲の細胞の増殖を促す現象。組織再生のメカニズムとして知られているが、本研究で示されたように、がん化のメカニズムにも転用されうる。
EdU 染色 / PH3 / MMP1 / JNK 経路
それぞれ細胞増殖や腫瘍浸潤を可視化するためのマーカー。EdU は DNA 合成中の細胞、PH3 は分裂期の細胞、MMP1 は組織浸潤、JNK 経路は炎症・浸潤シグナルの指標となる。
【参考リンク】
広島大学 千原研究室(細胞生物学研究室)(外部)
本論文の責任著者・千原崇裕教授が主宰する研究室。ショウジョウバエ遺伝学を駆使した研究を展開。
広島大学 大学院統合生命科学研究科(外部)
本研究の主要研究機関。基礎生物学プログラムとして千原研究室をはじめ多数の研究室が所属する。
EMBO Reports(論文掲載誌)(外部)
欧州分子生物学機構が発行する分子生物学分野の国際学術誌。Springer Nature 上で運営。
理化学研究所 生命機能科学研究センター(BDR)(外部)
共著者の小幡史明氏および佐久間知佐子氏の所属機関。本研究のアミノ酸定量解析を担当。
東北大学 大学院生命科学研究科(外部)
共著者の奥村美紗子氏の所属機関の一つ。生命科学研究の主要拠点として知られる。
【参考記事】
The Hippo paradox: how growth suppression drives tumor growth(News & Views 解説)(外部)
本論文の意義を解説した同日掲載の記事。pouch と hinge の応答差を Figure 1 で図解している。
Hippo-activated cells induce non-cell autonomous tumorigenesis in Drosophila(プレプリント版)(外部)
2025年5月公開の bioRxiv プレプリント版。査読を経て約1年後に EMBO Reports に正式掲載された。
The Hippo pathway kinases LATS1/2 suppress cancer immunity(Cell, 2016)(外部)
Hippo 経路が in vivo で腫瘍促進因子として働く事例を示したモロイシ氏らの先行研究。
Hippo pathway in cell–cell communication: emerging roles in development and regeneration(外部)
Hippo 経路の非細胞自律的機能と細胞間コミュニケーション役割を概説するレビュー論文。
Hippo Signaling at the Hallmarks of Cancer and Drug Resistance(Cells, 2024)(外部)
Hippo 経路発見の経緯と、がん治療標的としての併用療法の現状を概観するレビュー論文。
【関連記事】
30年来の生物学的謎が解決|クエオシン輸送体 SLC35F2 の発見で脳疾患・がん治療に新展開
SLC ファミリー輸送体ががん治療の新標的となり得ることを扱う記事。本記事の SLC36A1〜4 ファミリーへの言及と文脈が直接的に接続する。

転移性大腸がん、免疫療法が効かない理由を単一細胞解析で特定
腫瘍微小環境における細胞間「対話」を分子レベルで解読した研究。「がんは細胞単独の暴走ではなく近隣との対話の結果として起こりうる」という視座と重なる。
脳が守るか、脳が招くか。神経シグナルとがんの意外な関係【UC Merced 研究】
周囲の細胞・組織からの非細胞自律的シグナルががんに影響を及ぼす視点を扱う。本記事の発がんニッチ細胞概念と通底する。
【編集部後記】
Hippo 経路を標的とした薬は世界中で開発が進んでいますが、組織や部位によって効果が真逆に働く可能性が見えてきました。この発見は、皆さんが今後がん治療のニュースに触れる際の見方を、少し立体的にしてくれるはずです。
ショウジョウバエの研究が、なぜヒトのがんを理解する手がかりになるのか。そのスケール感の不思議さも含め、ぜひ皆さんなりに考えを巡らせてみていただけたら嬉しく思います。