がん免疫療法の世界で、「ブレーキを外す」発想から「ブレーキの効きを整える」発想への転換が始まっています。京都大学医学研究科のセオ・ウセオク准教授と西川博嘉教授らの研究グループは、PD-1遺伝子の発現を制御する「上流エンハンサー」というスイッチに着目し、ゲノム編集技術でこれを操作することで、PD-1を完全に消すのではなく「適度に調節」する新たなアプローチをマウスモデルで実証しました。その結果、攻撃役のT細胞が活性化してがんの増殖が顕著に抑制された一方、制御性T細胞の機能は維持され、自己免疫疾患のような副作用も認められませんでした。本成果2は2026年3月27日、国際学術誌「Immunology Letters」にオンライン掲載されています。
From: ![]() PD-1の適度な調節でがんを強力に抑制
PD-1の適度な調節でがんを強力に抑制
【編集部解説】
本研究は、京都大学医学研究科のセオ・ウセオク准教授と西川博嘉教授らによって発表されたものですが、その背景を理解するうえで欠かせない事実があります。PD-1は1992年に京都大学の本庶佑特別教授によって発見された分子であり、その発見は2018年のノーベル生理学・医学賞につながりました。本庶氏は現在、京都大学高等研究院特別教授であると同時に、京都大学がん免疫総合研究センターの初代センター長も務めており、本研究はまさにその系譜のなかから生まれた成果といえます。
共著者の西川博嘉教授は、国立がん研究センター研究所の腫瘍免疫研究分野長を本務とし、名古屋大学および京都大学にクロスアポイントメントで参画する、日本のがん免疫学を代表する研究者の一人です。基礎研究と臨床応用をつなぐ位置にいる人物であり、研究テーマの実装可能性を考えるうえで重要な布陣だといえます。
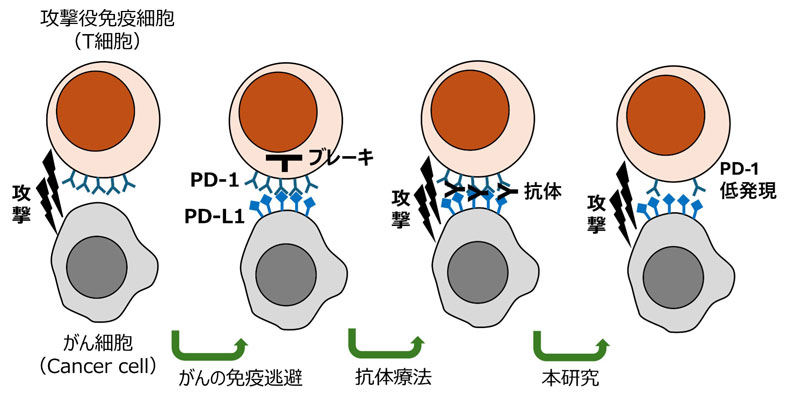
現在のPD-1阻害薬(オプジーボ、キイトルーダなど)はがん治療に革命をもたらしましたが、いくつかの課題も指摘されています。患者によって治療効果が大きく異なる点、そして自己免疫疾患のような副作用、いわゆる免疫関連有害事象が起こり得る点です。これは、PD-1のブレーキを「全部外してしまう」ことに伴う構造的な問題でもあります。
今回の研究の核心は「ブレーキを外す」のではなく「ブレーキの効きを調整する」という発想の転換にあります。遺伝子の発現量そのものを制御する「上流エンハンサー」と呼ばれるスイッチ領域に着目し、これをゲノム編集で操作することで、PD-1を完全に消すのではなく適度なレベルに保つという、これまでにないアプローチを示しました。
実は2024年にも、米国の研究グループがNature Immunology誌で類似のコンセプトを報告しています。それは慢性ウイルス感染における疲弊T細胞のPD-1発現を「中間レベル」に保つことで機能が最適化されるというもので、研究者らはこれを「スイートスポット」と呼びました。今回の京都大学の成果は、このアプローチがマウスモデルにおいてがん免疫の文脈でも成立することを示したわけで、エピジェネティック制御による免疫療法という方向性に説得力を加える結果といえるでしょう。
なぜこの「適度な調節」が重要なのでしょうか。PD-1には本来、免疫の暴走を防ぐ生理的な役割があります。完全に消失すれば自己免疫疾患のリスクが高まるのです。今回の研究で制御性T細胞の機能が維持されたという点は、まさにその懸念に応える結果であり、安全性と有効性の両立を示唆しています。
もっとも、この技術が実際の臨床応用に至るまでには相当な道のりが残されています。マウスでの結果がそのままヒトに当てはまる保証はありませんし、ゲノム編集を用いた治療は規制面での課題も大きい領域です。米国FDAが2023年12月に承認した世界初のCRISPR医薬品「Casgevy」のように、ex vivo(体外)での細胞改変なら現実味がありますが、安全性評価は慎重に行われる必要があります。
長期的な視点で捉えるなら、本研究は「免疫療法2.0」とでも呼ぶべき潮流の一翼を担うものです。抗体医薬による分子レベルの介入から、ゲノム編集による細胞レベルの精密制御へ。この移行が進めば、CAR-T細胞療法と組み合わせた次世代免疫細胞療法の設計や、副作用に悩む患者への新たな選択肢提供といった展開も視野に入ります。
今回の成果は単なる新しい治療法候補にとどまりません。生命科学が「壊す/消す」から「整える/調律する」へと向かう、より洗練されたパラダイムの萌芽として注目に値します。
【用語解説】
PD-1(Programmed Cell Death Protein 1)
T細胞などの免疫細胞表面に存在する分子で、免疫応答を抑える「ブレーキ」の役割を担う。1992年に京都大学の本庶佑特別教授によって発見された。がん細胞はPD-1を悪用してT細胞の攻撃から逃れるため、現代のがん免疫療法における最重要ターゲットとなっている。
上流エンハンサー(Upstream Enhancer)
遺伝子の発現量を調節するDNA配列のひとつで、対象となる遺伝子の上流領域に位置する。遺伝子の「スイッチ」または「アクセル/ブレーキの利き具合」に例えられ、ここを操作することで遺伝子そのものを破壊せずに発現量だけを調整できる。
ゲノム編集
特定のDNA配列を狙って改変する技術の総称。代表的な手法にCRISPR-Cas9があり、遺伝子の破壊・挿入・修正を高い精度で行える。本研究では、PD-1遺伝子の上流エンハンサーの破壊にこの技術が活用された。
制御性T細胞(Treg)
免疫応答の暴走を抑制し、自己免疫疾患を防ぐ司令塔のような役割を持つT細胞のサブセット。本研究で「制御性T細胞の機能が維持された」という結果は、副作用リスク低減の観点で極めて重要な意味を持つ。
免疫チェックポイント分子
免疫応答にブレーキをかける一連の分子の総称。PD-1のほか、CTLA-4、LAG-3などが知られる。これらを阻害する薬剤が「免疫チェックポイント阻害薬」と呼ばれる。
免疫関連有害事象(irAE)
免疫チェックポイント阻害薬の使用により発生する自己免疫様の副作用。皮膚障害、大腸炎、内分泌異常、肺臓炎など全身に及ぶ可能性があり、重篤化することもある。
疲弊T細胞(Exhausted T cell)
慢性的な抗原刺激にさらされ続けた結果、機能が低下したT細胞の状態。がんや慢性ウイルス感染で典型的に観察され、PD-1の高発現がその目印となる。
エピジェネティック制御
DNA配列そのものは変えずに、遺伝子の発現パターンを調整する仕組み。エンハンサーの活性化状態の変化はエピジェネティック制御の代表例である。
CAR-T細胞療法
患者自身のT細胞を体外で取り出し、がん細胞を狙撃するための受容体(CAR)を遺伝子工学的に組み込んだ上で体内へ戻す細胞療法。血液がんで特に高い治療効果が示されている。
【参考リンク】
京都大学(外部)
本研究を発表した日本を代表する研究大学。本庶佑特別教授によるPD-1発見の本拠地でもある。
京都大学がん免疫総合研究センター(CCII)(外部)
2020年発足のがん免疫研究拠点。本庶特別教授がセンター長を務め、西川教授もここに所属している。
本庶佑特別教授プロフィール(KUIAS)(外部)
2018年ノーベル生理学・医学賞受賞者。AIDやPD-1など主要な発見と業績がまとめられている。
Immunology Letters(Elsevier)(外部)
本研究成果が掲載された国際学術誌。欧州免疫学会連合(EFIS)の公式ジャーナルである。
Nature Immunology(外部)
免疫学分野のトップジャーナルのひとつ。PD-1エンハンサー関連の重要論文も掲載されている。
The Nobel Prize(Tasuku Honjo)(外部)
2018年ノーベル生理学・医学賞を受賞した本庶佑教授の公式プロフィールページ。
オプジーボ(小野薬品工業)(外部)
本庶教授の研究を基に開発された世界初のヒト型抗PD-1抗体医薬。小野薬品が共同開発した。
キイトルーダ(MSD)(外部)
MSD社が開発した抗PD-1抗体医薬。多くのがん種で承認されている代表的な免疫チェックポイント阻害薬。
FDA: First Gene Therapies for Sickle Cell Disease(外部)
2023年12月のCasgevy承認に関する米FDA公式発表。CRISPR/Cas9を用いた世界初の遺伝子治療薬。
【参考記事】
Epigenetic tuning of PD-1 expression improves exhausted T cell function and viral control(外部)
PD-1のエンハンサー欠失で発現を「スイートスポット」に保つマウス実験を報告したNature Immunology誌の論文。
The 2018 Nobel Prize in Physiology or Medicine – Press release(外部)
アリソン氏と本庶氏の共同受賞を伝える公式プレスリリース。1992年のPD-1発見の経緯を解説している。
Vertex and CRISPR Therapeutics Announce US FDA Approval of CASGEVY(外部)
2023年12月8日に米FDAが承認した世界初のCRISPR/Cas9ゲノム編集細胞療法に関する公式発表。
プロフィール:本庶 佑(KUIAS 京都大学高等研究院)(外部)
本庶佑特別教授の公式プロフィール。2017年の高等研究院特別教授就任の経緯などが確認できる。
西川 博嘉 教授(CCII 京都大学がん免疫総合研究センター)(外部)
本研究の共同研究者・西川博嘉教授のプロフィール。2024年7月のクロスアポイントメント着任が確認できる。
西川 博嘉 分野長(国立がん研究センター研究所)(外部)
西川教授の本務先である国立がん研究センター研究所のプロフィール。研究テーマと業績が確認できる。
【関連記事】
大阪大学・IFReCが牽引「制御性T細胞」発見と坂口志文氏のノーベル賞受賞|免疫学の革命と未来医療
本庶佑教授のPD-1と並び日本免疫学を象徴する坂口志文教授の制御性T細胞研究を扱った記事。本記事の「Treg機能維持」を理解する補助線となる。
2026年ブレークスルー賞発表—Casgevy・Luxturnaが証明した「遺伝子を治す時代」の幕開け
本記事の編集部解説で触れた世界初のCRISPR医薬Casgevyを深掘りした記事。ゲノム編集医療の現在地を俯瞰したい読者におすすめである。
転移性大腸がん、免疫療法が効かない理由を単一細胞解析で特定
ペムブロリズマブなど既存PD-1阻害薬の奏効率の限界(MSI-H 31〜55%、MSS 0〜3%)に踏み込んだ記事。本記事が論じる「現行PD-1阻害薬の課題」と直結する。
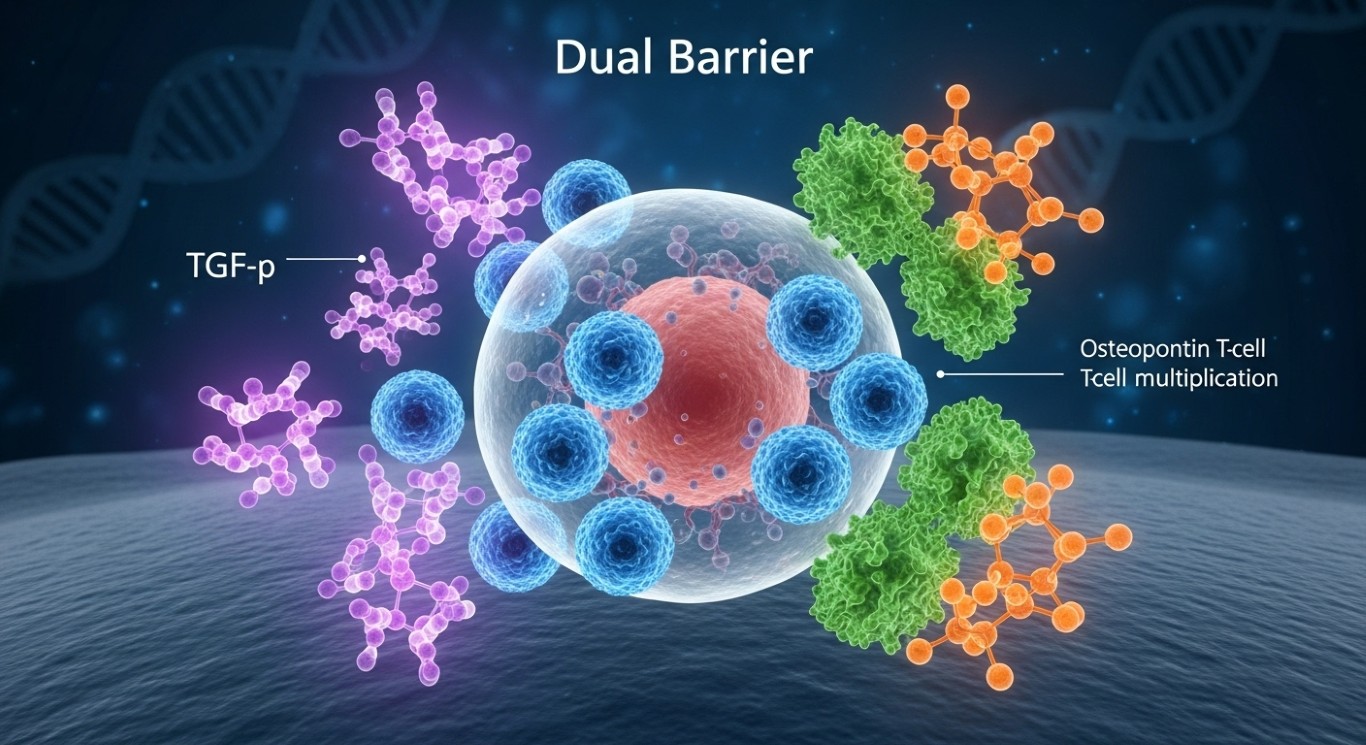
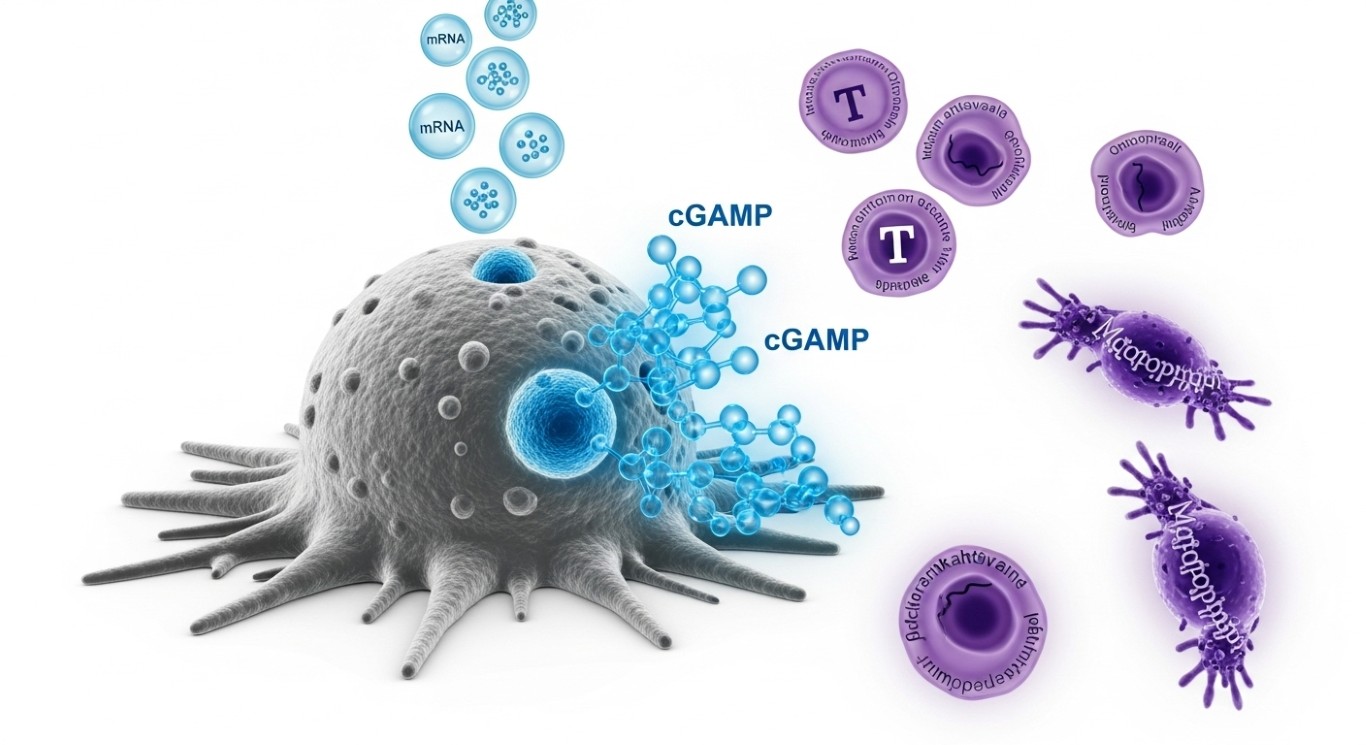
がん細胞を治療の工場に—MITが開発した次世代免疫療法、STING経路の革新的活性化方法
チェックポイント阻害剤との併用療法に踏み込んだMIT発の研究を紹介。本記事の「次世代免疫療法」の文脈と並走する内容である。
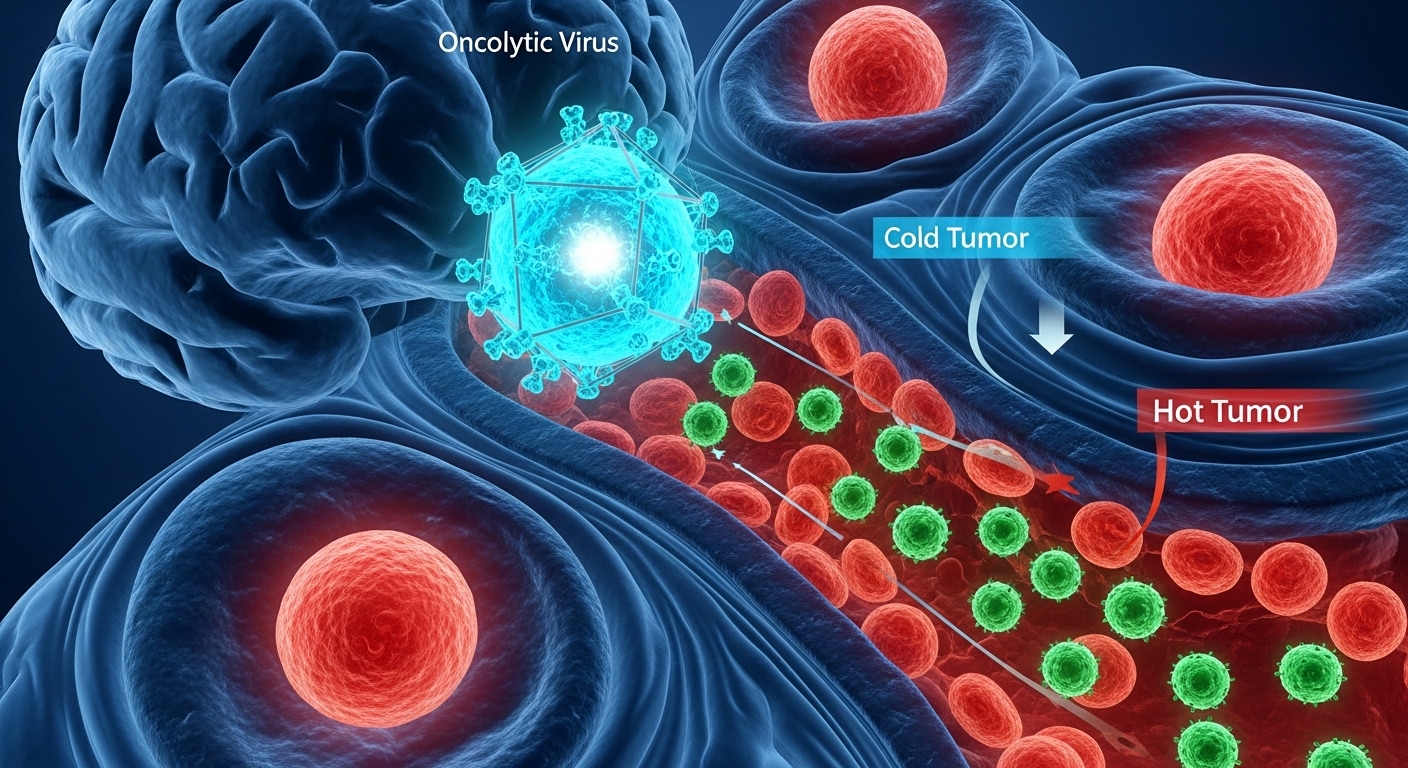
腫瘍溶解性ウイルスCAN-3110が膠芽腫に有効、Dana-FarberがCell誌で発表
免疫チェックポイント阻害剤との併用展望にも言及した臨床試験記事。「免疫療法2.0」というテーマで本記事と並走する。
AIとゲノム編集で「不治の病」は治療できる時代へ。アルツハイマー・がん・遺伝性疾患の最新治療法
CAR-T、Casgevy、ゲノム編集による次世代医療を総覧した記事。本記事の編集部解説をより広い文脈で捉えるための補強材料となる。

【編集部後記】
がんと向き合う場面は、誰にとっても他人事ではありません。PD-1の発見から30年以上が経ち、その本拠地・京都大学から「適度に調節する」という新しい発想が届けられたことに、編集部としても深い意味を感じています。
みなさんは医療における「やりすぎない技術」に、どんな可能性を感じるでしょうか。完全に消すのではなく、ちょうどよい量に保つ。この「調律」という考え方は、もしかするとがん治療だけでなく、自己免疫疾患や慢性感染症の領域にも広がっていくかもしれません。
身近な人がこの技術の恩恵を受ける日が来たとき、どんな選択肢が生まれているのか。一緒に未来の輪郭をたどっていけたら嬉しいです。