電極を脳に刺す——現在主流のブレインコンピューターインターフェース(BCI)が採用するこのアプローチに、根本的な疑問を投げかけるスタートアップがあります。元Neuralink共同創業者のMax Hodakが率いるScience Corporationは、体外で培養したニューロンを電子機器と融合させる「バイオハイブリッド型BCI」という独自路線を歩んでいます。そして今、その技術を初めて人間の脳で試す準備が整いつつあります。
Science Corporationは、バイオハイブリッド型BCIの米国初の臨床試験に向けて、イェール大学医学部神経外科学科長のMurat Günel博士をBCI担当医療ディレクターに迎えた。2021年創業の同社は先月、シリーズCで2億3,000万ドルを調達し、企業価値は15億ドルに達している。
Günel博士の役割は、培養ニューロンを組み込まない段階のセンサーを生きた人間の脳内に初めて設置し、安全性と有効性を評価することだ。対象となるのは、脳腫脹の処置などで大規模な脳手術が必要な患者で、センサーはNeuralinkのように脳組織に直接挿入するのではなく、脳の表面に載置される。同社はFDAへの承認申請なしに試験を進める方針であり、Günel博士は2027年の試験開始も「楽観的」との見方を示している。
From: ![]() Max Hodak’s Science Corp. is preparing to place its first sensor in a human brain
Max Hodak’s Science Corp. is preparing to place its first sensor in a human brain
📋 編集部注(2026年4月16日更新):本文中「Neuralinkは2024年に最初のヒト臨床試験(PRIMEスタディ)を開始」とあった箇所を修正しました(正確には「2023年5月にFDA承認を受けて開始し、最初の手術は2024年1月」)。あわせて、PRIMAのThe New England Journal of Medicine掲載論文の結果、および競合Precision NeuroscienceのFDAクリアランスに関する情報を追記しました。
【編集部解説】
「電極を脳に刺す」ことの代償——なぜ従来型BCIには限界があるのか
BCIという技術に対して、多くの人がまず思い浮かべるのはNeuralinkでしょう。細い電極を皮質に埋め込み、ニューロンの電気信号を読み取る——その映像的なインパクトがこの技術の代名詞になっています。2024年以降、ALS(筋萎縮性側索硬化症)や脊髄損傷の患者がNeuralinkのインプラントを使い、思考だけでパソコンを操作したり、画面上に言葉を生成したりすることに成功しています。
しかし、この「電極を脳に刺す」という方法には、構造的な弱点が潜んでいます。
脳は非常に繊細な臓器です。金属製の電極を組織内に挿入すると、脳は異物として認識し、「外来体反応(Foreign Body Response, FBR)」と呼ばれる免疫応答を起こします。具体的には、ミクログリア(脳の免疫細胞)が活性化し、電極の周囲にグリア瘢痕と呼ばれる組織が形成されます。この瘢痕は電極と周囲の神経細胞との間にバリアを作り、信号の読み取り精度を徐々に低下させていきます。
さらに、脳は頭蓋骨の中で絶えずわずかに動いていますが、硬い電極はその微動に追従できません。この「マイクロモーション」が慢性的な機械的損傷を引き起こし、電極周辺のニューロンが失われることも報告されています。
つまり、電極の本数を増やせばより多くの脳信号を拾えるのですが、本数を増やすほど脳組織へのダメージも増える——「チャネル数 vs 脳へのダメージ」というトレードオフが存在するのです。NeuralinkのN1インプラントは1,024チャネルという高密度を実現していますが、この数字を桁違いに増やすことは、現行の電極ベースのアプローチでは極めて困難です。
バイオハイブリッドという発想——「脳が受け入れるもの」をインターフェースにする
Science Corporationが取り組んでいるのは、このトレードオフそのものを解消しようという試みです。
同社のチーフサイエンスオフィサーであるAlan Mardinlyは、開発の出発点にある問いをこう表現しています——「100万個、あるいは1,000万個、脳に入れても傷つけないものは何か?」。その答えが、ニューロンそのものでした。
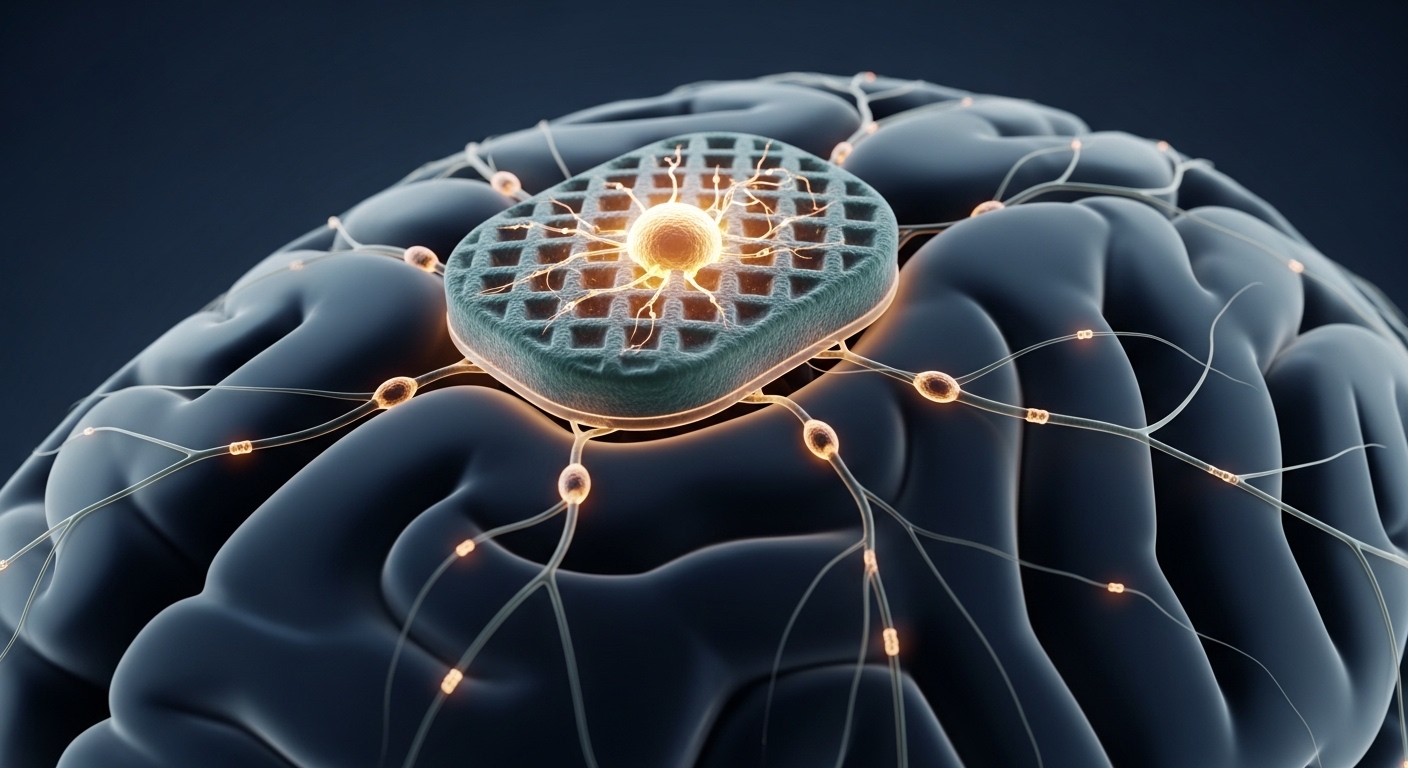
バイオハイブリッド型BCIの基本構造を整理しましょう。デバイスは「ワッフル状」の足場構造(マイクロウェル・スキャフォールド)を持ち、その中に体外で培養した光感受性ニューロンが収められています。このデバイスを脳の表面に載置すると、培養ニューロンの軸索(信号を伝えるケーブルに当たる部分)が脳組織の中へ自然に伸びていき、既存のニューロンとシナプス(化学的な接合部)を形成します。
ここで重要なのは、デバイス本体が脳を貫通しないという点です。電極を刺すのではなく、生きた細胞が自ら脳に「根を張る」。この違いが、先述した外来体反応のリスクを根本的に下げる可能性があります。
もうひとつの革新は、信号伝達に「光」を使うことです。培養ニューロンにはオプトジェネティクス(光遺伝学)の技術が適用されており、特定の波長の光パルスで刺激することができます。電気刺激は周辺の組織にも広がりやすいのに対し、光刺激はより精密なターゲティングが可能です。さらに、従来の電極が「電気チャネル」の数で帯域幅が決まるのに対し、バイオハイブリッド型では100万個のニューロンを移植すれば10億を超えるシナプスが形成されうると同社は推計しています。「チャネル」という概念そのものを超えた、桁違いの帯域幅が理論上は実現しうるわけです。
2024年のマウス実験——何が分かり、何がまだ分からないのか
2024年11月、Science Corporationの研究チームはプレプリント論文をbioRxivに公開しました。この論文では、光感受性ニューロンを搭載したバイオハイブリッドデバイスをマウスの大脳皮質に埋め込み、以下の成果が報告されています。
移植されたニューロンは数週間にわたって生存し、自発的な神経活動を示しました。埋め込み3週間後の時点で、およそ半数の光感受性ニューロンが生き残っていたとIEEE Spectrumは報じています。さらに、マウスはデバイスからの光刺激を知覚し、それに基づいて目標志向行動(報酬を得るための左右の選択)を実行することに成功しました。
ただし、見過ごしてはならない点があります。バイオハイブリッドデバイスを装着した9匹のマウスのうち、4匹はこのタスクを学習できなかったのです。なぜ成功率にばらつきが出るのか——この原因は論文の中で十分に解明されていません。また、この実験で使われたのは同系統のマウス由来の細胞であり、人間のiPS細胞(人工多能性幹細胞)から作った培養ニューロンが同様にうまく機能するかは、まだ実証されていません。
研究チーム自身も、移植ニューロンがホスト脳にどの程度「統合」されたのかを正確に測定する難しさを認めています。これはマウスでの初期段階の概念実証であり、人間の脳での有効性は未知数です。
FDA承認なしの臨床試験——その論理と疑問点
今回のニュースで最も議論を呼びそうなのが、Science CorporationがFDAへの承認申請なしに臨床試験を実施する方針を示していることです。
米国の医療機器規制では、臨床試験に使われるデバイスは「重大リスク(Significant Risk, SR)」と「非重大リスク(Nonsignificant Risk, NSR)」に分類されます。SRデバイスはFDAへのIDE(治験用機器免除)申請が必要ですが、NSRデバイスの場合はIRB(施設内倫理審査委員会)の承認のみで臨床試験を開始できます。
Science Corporationは、同社のセンサーがNeuralinkのように脳組織を貫通せず、脳の表面に載置するだけであるため、NSRに該当すると説明しています。少なくともTechCrunchの取材に対してはそのような根拠を示しており、FDAへの承認申請を行わない方針を明らかにしています。確かに、脳実質を貫通しないという点では、侵襲性はNeuralink型よりも低いと言えるかもしれません。
しかし、FDAのガイダンスによれば、「インプラント」として使用されるデバイスは原則としてSRに分類されます。頭蓋骨を開けて脳の表面にセンサーを置く行為が「非重大リスク」と見なされるかどうかは、自明ではありません。最終的なリスク判定はIRBが行いますが、FDAがこの判断に異議を唱える権限を持っている点には留意が必要です。
また、対象となる患者は「すでに大規模な脳手術が必要な人」であり、脳腫脹の処置で開頭が予定されている脳卒中患者などが想定されています。実際、このアプローチには合理性があります。なぜなら頭蓋骨が開かれる手術の機会を利用すれば、追加の外科的侵襲は最小限に抑えられるからです。ただし逆に言えば、このような限定された条件下でしかデータを取れないということは、将来的に健康な人も含む広範な適用を目指す場合、別途FDAの正式な承認プロセスを経ることが不可避になるでしょう。
この戦略がどう評価されるかは、ニューロテクノロジー業界全体の規制環境にも影響を与えます。イノベーションの加速と患者保護のバランスを、どの地点で取るのか、Science Corporationの判断は、ひとつのテストケースになりうるものです。
【2026年4月16日 追記】
この文脈で参照に値するのが、競合・Precision Neuroscience(2021年創業)の事例です。同社は1,024電極を薄型フィルムに埋め込んだ皮質表面電極アレイ「Layer 7 Cortical Interface」を開発しており、Science Corporationと同様に「脳に刺さず、皮質表面に置く」設計を採っています。2025年4月17日、PrecisionはこのLayer 7に対してFDA 510(k)クリアランスを正式取得しました——次世代ワイヤレスBCIを開発する企業として初の正式なFDAクリアランスとされています。最大30日間の留置が承認されており、術中脳マッピングなどに活用されます。皮質表面デバイスで正式クリアランスを取得したPrecisionと、同様の設計でFDA申請なし(NSR判断)を選択したScience Corporationの対比は、今後のBCI規制の「型」を決める重要な問いを投げかけています。
パーキンソン病への展望——「症状の制御」から「進行の停止」へ
Günel博士が特に期待を寄せているのが、パーキンソン病への応用です。その理由を理解するには、現在の治療法の限界を知る必要があります。
パーキンソン病は、中脳のドーパミンを産生するニューロンが徐々に失われていく進行性の疾患です。初期にはドーパミン補充薬(レボドパなど)で症状を管理できますが、病気が進むにつれて薬の効果は低下し、運動合併症が顕著になります。
進行期の治療として現在広く行われているのが深部脳刺激(DBS)です。脳の深部に電極を挿入し、電気パルスで異常な神経活動を抑制する手法で、特に振戦(手足のふるえ)に効果があります。しかし重要なのは、DBSは症状を緩和するものであって、ドーパミンニューロンが失われていく根本的なプロセスを止めるものではないということです。
一方、もうひとつの実験的アプローチとして注目されているのが、幹細胞由来のドーパミンニューロンを脳内に移植する「細胞補充療法(Cell Replacement Therapy, CRT)」です。失われた細胞を補い、ドーパミンの持続的な供給を回復させることで、根本的な治療につながる可能性が指摘されています。しかし現時点では、移植細胞の生着率のばらつき、移植に伴う不随意運動(ジスキネジア)の発生、そして移植細胞自体に病変が広がるリスクなど、多くの課題が残されています。
Günel博士が描く構想は、バイオハイブリッドBCIによって「電子的な制御」と「生物学的な修復」を一体化するというものです。電極で振戦を抑えるだけでなく、移植した培養ニューロンが失われた回路を補完し、病気の進行そのものを食い止める——理論的には、DBSと細胞移植の「いいとこ取り」ができる可能性があります。
ただし、これはまだ構想の段階です。バイオハイブリッドデバイスで中脳の深部にある特定の神経回路を標的にできるのか、培養ニューロンがドーパミン産生細胞として機能するのか、長期的に安定した効果が得られるのか——いずれもこれから検証すべき問いです。
培養ニューロンを脳に入れるということ——安全性の未知数
バイオハイブリッド型BCIの独自性は、同時にその最大の未知数でもあります。生きた細胞を脳に導入するという行為は、電子デバイスの埋め込みとは質的に異なるリスクを伴います。
Science Corporationは、移植した幹細胞が制御不能に増殖するリスクに対処するため、「キルスイッチ」を設計していると報じられています。この安全機構は、抗ウイルス薬のガンシクロビルを「目的外使用」することで、移植細胞を選択的に除去できる仕組みです。HSV-TK(ヘルペス単純ウイルスチミジンキナーゼ)遺伝子を組み込んだ細胞にガンシクロビルを投与すると、細胞死が誘導されるという技術で、幹細胞治療の安全機構として広く研究されています。
しかし、この分野の研究文献を見ると、キルスイッチの有効性は万全ではありません。in vitroでは機能しても、生体内(in vivo)では十分に腫瘍形成を防げなかったという報告もあります。加えて、HSV-TK自体がヒトの免疫系にとって異物として認識される(免疫原性がある)可能性も指摘されています。
もっとも、今回計画されている最初の臨床試験では、培養ニューロンはまだ搭載されません。まずはセンサー部分の安全性と計測性能を確認するフェーズです。培養ニューロンの安全性が本格的に問われるのは、その後のステップになります。
BCI市場の中でのScience Corporation——Neuralinkとは異なる時間軸
BCI業界全体を俯瞰すると、Science CorporationとNeuralinkは異なるフェーズにいることが分かります。
Neuralinkは2023年5月にFDA承認を受けてPRIMEスタディを開始し、同年秋から患者募集を始め、2024年1月に最初の手術を実施しました。その後、2026年1月時点で試験参加者は21名に拡大したと報じられています。2025年5月にはFDA Breakthrough Device Designation(突破口機器指定)を言語回復用途で取得し(商業販売承認は未取得)、2025年のシリーズEで6億5,000万ドルを調達、企業価値は約90億ドル規模(2025年6月時点、pre-money)に達しています。すでに複数名の被験者でデータを取得できる段階にあります。
対するScience Corporationは、企業価値15億ドル、まだセンサー単体の臨床試験すら始まっていない段階です。完全版のバイオハイブリッドデバイスの臨床試験はさらに先の話であり、Günel博士はセンサーだけの試験ですら2027年開始は「楽観的」としています。
しかし、この「遅さ」を単純にネガティブに捉えるべきではないかもしれません。Science Corporationが取り組んでいるのは、BCIの根本的なアーキテクチャを変えることです。2024年のBCI分野への累計VC投資額は約23億ドルに達しますが、その大半は電極ベースの技術に立脚しています。バイオハイブリッド型という選択肢が実証されれば、産業全体の技術的前提が変わる可能性があります。
同社はすでにPRIMAという視力回復デバイスで臨床試験と規制対応の実績を積んでいます。PRIMAは2023年にFDAのBreakthrough Device指定を受けており、こうした実績が将来のバイオハイブリッドBCIの規制プロセスを進める際の基盤になると考えられます。
しかし市場での位置づけより先に、技術そのものについてまだ答えが出ていない問いがある——それが次のセクションで整理する論点です。
【2026年4月16日 追記】
PRIMAの規制上の実績を具体的に示すデータが、2025年10月に公開されています。Science Corporationは同月、PRIMAの臨床試験(PRIMAvera)の結果をThe New England Journal of Medicine(NEJM)に発表しました(誌面掲載は2026年1月15日号)。欧州5か国・17施設で実施されたこの試験では、加齢黄斑変性による地図状萎縮で中心視野を失った38名の患者を対象とし、80%以上が有意な視力改善を達成、文字・数字・単語を読めるようになったと報告されています。データ安全性モニタリング委員会(DSMB)はリスク対効果比がプラスと結論づけ、欧州市場承認を推奨しており、2026年中のCEマーク取得が見込まれています。これはバイオハイブリッドBCIへの道を歩む前に、Science Corporationが世界最高峰の医学誌に査読済みの臨床エビデンスを積み上げていることを意味します——規制当局との信頼構築において、無視できない実績です。
まだ見えないもの——誠実に線を引く
ここまで見てきた通り、バイオハイブリッドBCIの構想は知的に魅力的であり、技術的な合理性も感じられます。しかし、分かっていることよりも、まだ分かっていないことの方がはるかに多い段階であることも、率直に認めるべきでしょう。
まだ答えが出ていない主要な問いを整理します。
まず、ヒトiPS細胞由来の培養ニューロンが、マウスの同系統細胞と同じようにホスト脳と統合するかは未実証です。ヒトとマウスでは免疫環境も大きく異なります。次に、移植ニューロンの長期的な安定性——数年、数十年単位で機能し続けるかどうかは、まだ誰にも分かりません。さらに、脳の表面に載置する方式でパーキンソン病に必要な深部の標的回路にどう到達するのかという空間的な課題も、今後の研究で解決すべきテーマです。
Science Corporationの挑戦は、「脳を傷つけずに脳とつながる」という、BCIが最初からずっと向き合ってきた根源的な問いに対する、ひとつの答えの試みです。その答えが正しいかどうかは、これからの科学が決めることになります。その判断の最初の節目となるのは、2027年以降に予定されるセンサー単体の安全性試験です。そこから得られるデータが、バイオハイブリッドという選択肢の実現可能性を示す最初の証拠になります。
【用語解説】
バイオハイブリッドBCI(Biohybrid BCI)
体外で培養したニューロン(神経細胞)と電子回路を組み合わせたBCI。従来の金属電極に代わり、生きた細胞を脳との「橋渡し役」として使う。細胞体はデバイス側に留め、軸索(信号伝達の突起)だけを脳組織に伸ばして既存ニューロンとシナプス結合させる設計。
オプトジェネティクス(光遺伝学)
光感受性タンパク質(チャネルロドプシンなど)の遺伝子を特定のニューロンに導入し、光パルスで神経活動をミリ秒単位で制御する技術。スタンフォード大学のKarl Deisseroth博士らが2000年代に確立。電気刺激より細胞種を選んで標的化できる点が特長。Science Corporationの培養ニューロンはこの技術を応用して光で駆動される。
外来体反応(Foreign Body Response, FBR)
生体が異物(金属電極など)を認識した際に起こす免疫応答。ミクログリア(脳の免疫細胞)が活性化し、電極周囲にグリア瘢痕を形成。これが電極と周囲ニューロンの間に絶縁バリアを作り、長期的に信号計測精度を低下させる。従来型BCIの耐久性を制約する主因のひとつ。
グリア瘢痕(Glial scar)
脳が損傷や異物に反応して形成する瘢痕組織。アストロサイトやミクログリアが集積して構成される。神経回路の再生を妨げる一方、感染拡大を防ぐ保護的役割も持つ。電極インプラントの長期的な機能劣化の主要因として研究されている。
マイクロウェル・スキャフォールド
Science Corporationのバイオハイブリッドデバイスが採用する「ワッフル状」の微細な穴(ウェル)構造の足場。この穴の中に培養ニューロンを格納し、軸索だけを脳組織へと伸ばす設計。細胞体を安定保持しながら生物学的統合を促す役割を担う。
深部脳刺激(DBS:Deep Brain Stimulation)
脳の深部(基底核や視床下核など)に電極を植え込み、持続的な電気パルスで異常な神経活動を抑制する手術療法。パーキンソン病の振戦や本態性振戦、ジストニアに有効。ただし病気の進行を止める効果はなく、症状緩和が主目的。
細胞補充療法(CRT:Cell Replacement Therapy)
失われた特定の神経細胞(パーキンソン病ではドーパミンニューロンなど)を、体外で培養・分化させた幹細胞由来の細胞で補う治療法。根本治療への可能性を持つが、生着率のばらつきや移植ジスキネジア、免疫拒絶などの課題が残る研究段階の治療。
iPS細胞(人工多能性幹細胞)
皮膚や血液などの体細胞に特定の転写因子を導入して初期化し、さまざまな細胞に分化できる状態に戻した幹細胞。2006年に京都大学・山中伸弥教授が樹立(2012年ノーベル生理学・医学賞)。患者自身の細胞から作れるため免疫拒絶リスクを低減できる点が特長。バイオハイブリッドBCIでは、移植するニューロンの製造元として中心的な役割を担う見込み。
IDE(Investigational Device Exemption)
米FDA(食品医薬品局)が未承認医療機器の臨床試験を許可するための「治験用機器免除」申請制度。「重大リスク(SR)」に分類されるデバイスはIDE申請が必須。承認を得た上でFDAの監督下で臨床試験を実施する。
NSR / SR(非重大リスク / 重大リスク)
臨床試験に使用する医療機器のリスク分類。SR(Significant Risk)デバイスはFDAへのIDE申請が必要。NSR(Nonsignificant Risk)デバイスはIRBの承認のみで試験開始可能。インプラントは原則SRとされるが、Science Corporationは今回の皮質表面センサーをNSRと主張している。
IRB(施設内倫理審査委員会)
Institutional Review Board。大学・病院などの研究機関に設置され、人体を対象とする研究の倫理的妥当性と参加者の安全性を審査・承認する委員会。NSRデバイスの臨床試験はIRBの承認のみで実施できる。
キルスイッチ(自殺遺伝子システム)
移植細胞が制御不能に増殖(腫瘍化)するリスクに備え、外部からの薬剤投与で移植細胞を選択的に除去できる安全機構。幹細胞治療の安全管理として研究が進む。Science Corporationはガンシクロビルを用いるHSV-TK系のキルスイッチを採用していると報じられている。
HSV-TK / ガンシクロビル
HSV-TK(ヘルペス単純ウイルスチミジンキナーゼ)は、ウイルス由来の酵素遺伝子。この遺伝子を組み込んだ細胞にガンシクロビル(抗ウイルス薬)を投与すると、薬が細胞毒に変換されて細胞死を誘導する。幹細胞由来の移植細胞の自殺遺伝子システムとして活用されるが、in vivoでの効果や免疫原性には課題も残る。
シナプス
ニューロン同士が信号を伝え合う接合部。電気信号が軸索末端に達すると、神経伝達物質が放出され、接続先のニューロンの受容体に結合して信号を伝える化学的シナプスが主流。バイオハイブリッドBCIの移植ニューロンは、ホスト脳のニューロンとシナプスを形成することで「自然な統合」を実現しようとする。
軸索(アクソン)
ニューロンの細長い突起で、電気信号(活動電位)を細胞体から離れた場所へ伝導するケーブルに相当する構造。一つのニューロンは一本の軸索を持ち、その末端から他のニューロンにシナプスを介して信号を送る。バイオハイブリッドデバイスでは、培養ニューロンの軸索がデバイス外へ伸長してホスト脳組織に統合されることが重要な機能要件。
【参考リンク】
Science Corporation(公式サイト)(外部)
企業概要・製品情報・採用情報・研究成果を網羅。BCIの現在地と同社のミッションをまず把握するための出発点。
Science Corporation|バイオハイブリッド技術ページ(外部)
バイオハイブリッド型BCIの技術原理、チャネル数の考え方、マイクロウェル構造の仕組みを図解で解説した公式技術ページ。
Science Corporation|公式ブログ「Biohybrid Neural Interfaces」(外部)
Hodak CEOらによる公式解説(2024年11月)。100万ニューロンで10億超シナプスの根拠やオプトジェネティクス採用の意義を詳述。
Neuralink(公式サイト)(外部)
電極型BCIの代表格。バイオハイブリッド型との技術的・戦略的違いを比較する上での参照先。
Murat Günel博士|イェール大学医学部プロフィール(外部)
Günel博士の専門領域と研究実績、イェール大学での役職を確認できる公式プロフィールページ。
bioRxivプレプリント|Brown et al. (2024)(外部)
2024年11月公開のマウス実験論文(査読前)。バイオハイブリッドデバイスの埋め込み実験データを確認できる一次情報源。
Parkinson’s Foundation(パーキンソン財団)(外部)
米国最大のパーキンソン病患者支援団体。DBS解説や最新の臨床試験情報、患者コミュニティへの参加窓口を含む。
ClinicalTrials.gov|BCI関連試験一覧(外部)
進行中・募集中のBCI関連試験を一覧できる国立衛生研究所の臨床試験登録データベース。
Subretinal Photovoltaic Implant to Restore Vision in Geographic Atrophy Due to AMD — The New England Journal of Medicine(外部)
2025年10月20日発表・2026年1月15日誌面掲載。PRIMAの欧州臨床試験(PRIMAvera)の査読済み結果論文。38名のデータ、12か月にわたる視力改善エビデンスを確認できる一次情報源。
Precision Neuroscience receives FDA clearance for brain implant — MedTech Dive(外部)
2025年4月17日付。Layer 7 Cortical InterfaceへのFDA 510(k)クリアランスの詳細と、37名での臨床試験データ。Science Corporationの規制戦略との対比を考える際の参照先。
【参考記事】
Science Corp’s Biohybrid BCI Adds Neurons to the Brain — IEEE Spectrum(外部)
マウス実験の技術的詳細(ワッフル状構造・ニューロン生存率・9匹中4匹が未学習)を最も正確かつ詳細に報じた記事。
Neuralink Rival’s Biohybrid Implant Connects to the Brain With Living Neurons — Singularity Hub(外部)
2024年11月のプレプリント発表時の文脈と業界の反応をまとめた記事。Neuralinkとの技術的対比を分かりやすく整理。
Science Corporation Prepares First U.S. Trials of Biohybrid Brain Interface — Prism News(外部)
今回の発表を詳細に報じた速報記事。PRIMAの臨床データやNeuralinkのPRIMEスタディとの比較を含む。
Computer Chips in Our Bodies Could Be the Future of Medicine — TIME(外部)
キルスイッチ(ガンシクロビルを使った自殺遺伝子システム)の存在を報じた記事(2025年11月)。購読が必要な場合あり。
The Brain-Computer Interface Is A Really Near Thing — 21st Century Tech Blog(外部)
BCI市場の全体像(約250社・累計約23億ドルのVC投資)を示したデータを含む記事。
bioRxivプレプリント:Brown et al. (2024)|A biohybrid neural interface…(外部)
2024年11月公開のマウス実験論文(査読前プレプリント)。移植ニューロンの生存・行動変容の実験データを記録した一次情報源。
【編集部後記】
脳を傷つけずに脳とつながりたい——BCIの歴史は、この矛盾との格闘そのものだったのかもしれません。生きた細胞に橋渡しを託すという発想は素晴らしいです。しかし、マウス9匹中4匹が学習できなかった現実や、FDA承認なしという判断が投げかける問いも、この技術を実現させる難しさを表しています。「2027年でも楽観的」というGünel博士の言葉もありましたが、この先に何が見えてくるのか。続報を待ちたいと思います。